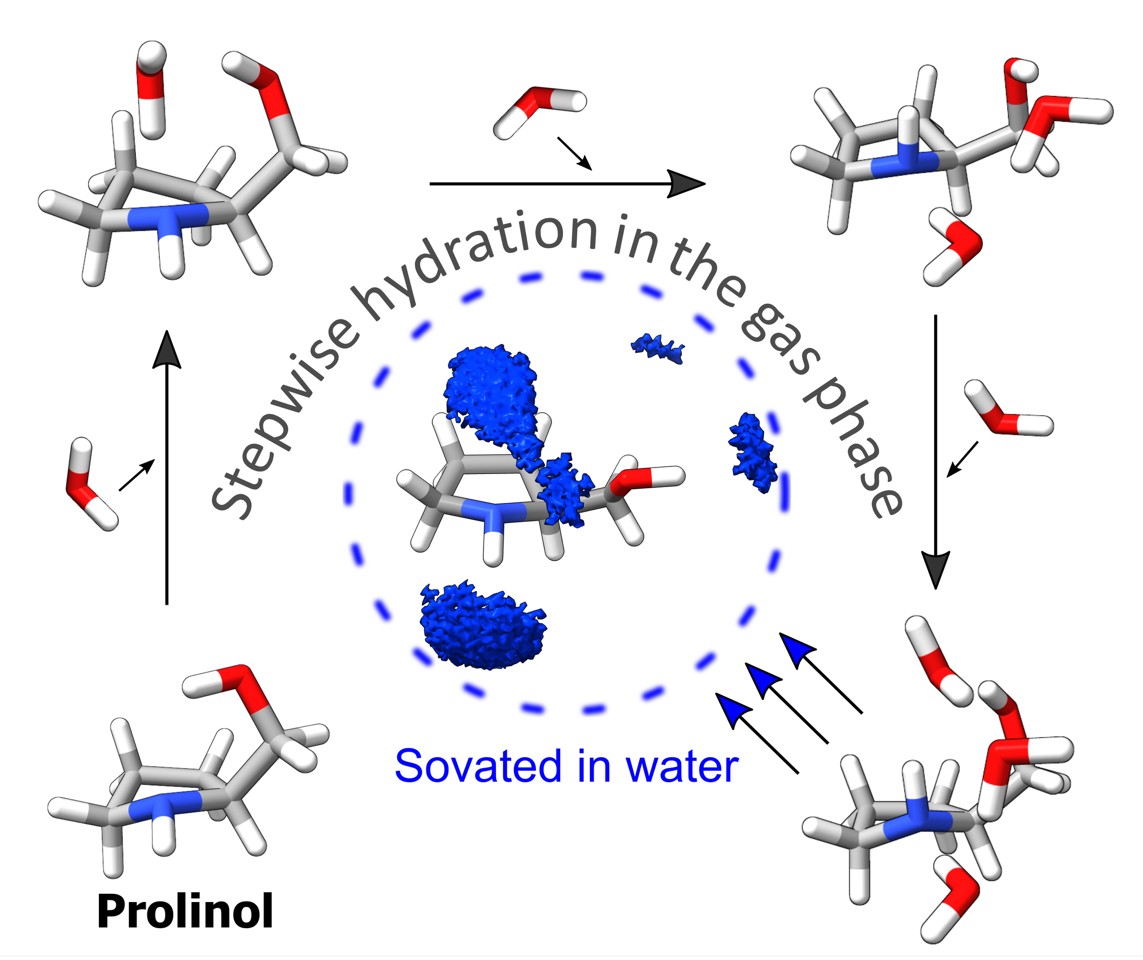
Una investigación desarrollada por el Grupo de Espectroscopía de la EHU y del Instituto Biofisika (CSIC/EHU), y publicada en la prestigiosa revista Journal of the American Chemical Society, ha analizado la hidratación gradual del prolinol, una molécula utilizada ampliamente como catalizador y como bloque de construcción en síntesis química. El estudio demuestra que unas pocas moléculas de agua son capaces de cambiar completamente la estructura preferida del prolinol.
La Sociedad de Biofisica de España destaca un trabajo del Grupo de Espectroscopía de la EHU
El estudio ayuda a comprender cómo el agua puede modificar la estructura de las moléculas y afectar a procesos clave como la catálisis o el reconocimiento molecular en sistemas biológicos
- Investigación
Fecha de primera publicación: 30/01/2026
La Química Física aplica los principios y conceptos de la física para comprender los fundamentos de la química y explicar cómo y por qué ocurren las transformaciones de la materia a nivel molecular. Una de las ramas de este campo se centra en entender cómo cambian las moléculas a lo largo de una reacción o de un proceso químico.
Comprender las interacciones de las moléculas quirales con el agua es fundamental, dado el papel central que desempeña este solvente en procesos químicos y biológicos. Las moléculas quirales son aquellas que, aun estando formadas por los mismos átomos, no pueden superponerse con su imagen especular, de forma similar a lo que ocurre con las manos derecha e izquierda o con un par de zapatos.
En este contexto, el Grupo de Espectroscopía de la EHU y del Instituto Biofisika (CSIC/EHU), liderado por Emilio J. Cocinero, ha investigado las interacciones del prolinol (un catalizador quiral y auxiliar ampliamente utilizado en la síntesis asimétrica) con una, dos y tres moléculas de agua. El estudio se enmarca en la línea de investigación del grupo centrada en el análisis estructural de moléculas relevantes mediante técnicas espectroscópicas de alta resolución, y ha sido recientemente destacado por la Sociedad de Biofísica de España (SBE).
“Este trabajo ha permitido conectar tres escalas que normalmente se estudian por separado: la molécula aislada, la microsolvatación con unas pocas moléculas de agua y el comportamiento en disolución”, explica Emilio J. Cocinero, investigador de la EHU y del Instituto Biofisika (CSIC/EHU).
Los resultados muestran de forma directa que el agua no actúa únicamente como un ‘medio’ pasivo, sino que puede desempeñar un papel activo en la forma que adoptan las moléculas. “Observamos que unas pocas moléculas de agua son capaces de cambiar completamente la estructura preferida de una molécula quiral. Esto es relevante porque la forma de una molécula condiciona cómo reconoce a otras, cómo reacciona o cómo funciona en un entorno biológico o químico”, señala Cocinero.
El prolinol es una molécula pequeña pero muy representativa. Se utiliza ampliamente como catalizador y como bloque de construcción en síntesis química, y además contiene dos grupos funcionales clave (un alcohol y una amina) que interactúan fuertemente con el agua. Esto lo convierte en un modelo ideal para estudiar cómo el agua compite con los enlaces internos de la molécula y puede forzar cambios estructurales. Además, su estructura flexible permite observar con claridad los efectos inducidos por la hidratación. “Al añadir agua paso a paso, observamos que el prolinol adopta conformaciones que en condiciones normales serían ‘desfavorables’. El agua actúa como un verdadero ‘interruptor conformacional’ ”, añade el investigador.
Además, el estudio se apoya en un enfoque experimental que combina espectroscopía rotacional de muy alta resolución con cálculos teóricos y estudios en disolución mediante RMN y simulaciones. Esta combinación permite conectar con gran detalle lo que ocurre cuando solo unas pocas moléculas de agua interactúan con el prolinol y el comportamiento real de la molécula en disolución. “Para entender cómo funcionan las moléculas en agua, a veces basta con mirar con lupa qué hacen solo dos o tres moléculas de solvente. Creemos que esta idea es relevante para muchos otros sistemas químicos y biológicos”, concluye.
Información complementaria
El estudio ha sido realizado en colaboración con el Departamento de Química del King’s College London, del Departamento de Química de la Universidad de Virginia, del Instituto de Química Orgánica General (IQOG-CSIC) en Madrid, del Departamento de Química y del Instituto de Investigación en Química (IQUR) de la Universidad de La Rioja.
Referencia bibliográfica
- Stepwise Hydration Reveals Conformational Switching in Chiral Prolinol
- Journal of the American Chemical Society
- DOI: 10.1021/jacs.5c13582